Минздрав России одобрил клинические исследования препарата от ботулизма
Об этом заявил глава ведомства. Глава Министерства здравоохранения России Михаил Мурашко заявил,
Об этом заявил глава ведомства.
Глава Министерства здравоохранения России Михаил Мурашко заявил, что ведомство дало разрешение на проведение клинических исследований нового препарата для нейтрализации токсина ботулизма А. сообщает RT со ссылкой на РИА Новости.
«Минздрав России выдал разрешение на клинические исследования нового препарата для нейтрализации токсина ботулизма А, разработанного НИЦЭМ имени Гамалеи», — сообщил Мурашко.
Как уточнил министр, речь идет о лекарстве на основе моноклональных антител, которые могут связывать токсин в крови больного.
По словам Мурашко, на доклиническом этапе проведены исследования токсичности, безопасности, эффективности на моделях, где препарат показал хорошие результаты.
Источник: sibdepo.ru Фото: freepik.Последние новости

В России решили регулировать прием в вузы на платное обучение
Скоро. Председатель Совета Федерации Валентина Матвиенко и сенаторы подписали законопроект о государственном регулировании платного приема в вузы, который скоро будет внесен в Госдуму.

Компенсация морального вреда и имущественный ущерб за смерть питомца
Заводским районным судом г. Новокузнецка рассмотрено гражданское дело по иску Б. о взыскании с ответчика А.
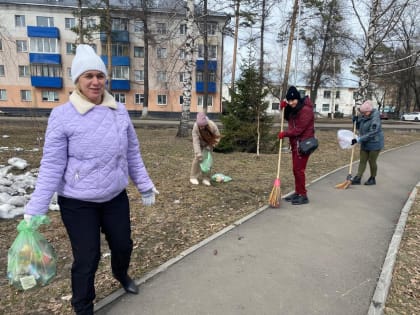
Сегодня, 4 апреля, мысковчане активно вышли на Всекузбасский субботник, посвященный 80-летию Победы в Великой Отечественной войне
Этот день собрал людей разных возрастов и профессий, объединенных общей целью — сделать родной город чище и красивее.

Куда пойти с детьми в Уфе: 10 весёлых мест на выходные
Идеи для семейного отдыха в столице Башкортостана — от активных игр до познавательных музеев